L'examen clinique
Il se décompose en trois temps :
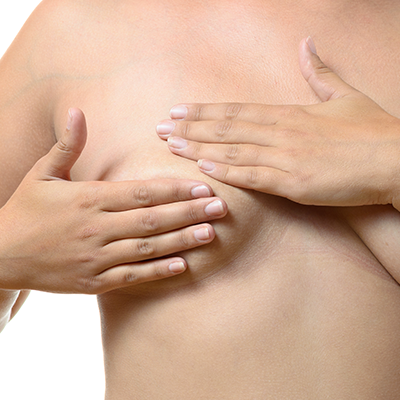
1 – L’observation clinique
- Au niveau cutané par la recherche d’une lésion comme une ulcération, une inflammation ou d’une rétractation,
- Au niveau du mamelon, à la recherche d’un écoulement mammaire ou d’une rétractation mamelonnaire.
2 – La palpation des deux seins
La masse perçue, sa taille, sa localisation dans le sein, l’identification de sa nature (souple ou ferme, douloureuse ou non, adhérente à la peau ou non)
3 – La palpation des aires ganglionnaires au niveau axillaire, et sus claviculaire
Le but est de rechercher des ganglions, leur nombre, leur adhésion à la peau ou au tissu de voisinage
À ce stade, la poursuite de l’investigation sera évaluée par le médecin.
La mammographie
C’ est une radiographie des seins. L’examen est réalisé debout ; le sein est comprimé et deux clichés sont pris en incidence de face et en incidence oblique.
Le médecin commentera les images et proposera éventuellement un examen échographique complémentaire si nécessaire. Une tumeur se traduit par une masse plus ou moins régulière associée parfois à de petites taches blanches appelées micro calcifications. Ces dernières en fonction de leurs nombres, de leurs formes, de leur répartition feront suspecter l’existence ou non d’un cancer.
Les examens complémentaires
1 – Les examens d’imagerie
- L’échographie : elle utilise des ultrasons, alors que la mammographie des rayons X. Cet examen est totalement indolore, les seins ne seront pas comprimés. Elle permet de différencier une masse liquidienne (kystes), d’une masse tissulaire (tumeur).
- L’IRM (Imagerie à résonance magnétique) est le dernier examen radiologique qui peut être effectué. Il n’est pas systématique, mais il sera utile devant une suspicion d’anomalie bénigne ou maligne.
2 – L’examen anatomopathologique
Un fragment de tissu sera prélevé et analysé au microscope afin de confirmer la nature de la lésion.
Les techniques de prélèvement
1 – La cytoponction
La cytoponction à l’aiguille, peut- être faite lors de la consultation, par le médecin, avec une aiguille fine. Cet examen ne prélève que quelques cellules qui seront examinées au microscope. Cette technique est de moins en moins utilisée au profit des biopsies. Elle peut être utile dans le cas de cytoponction d’image d’allure bénigne ou des ganglions axillaires.
2 – Les biopsies
Les biopsies prélèvent des fragments de tissu et sont réalisées à travers la peau par un groupe d’aiguilles soit par micro ou macro biopsies. Elles sont réalisées en ambulatoire (pas d’hospitalisation) avec une anesthésie locale.
- La micro-biopsie : elle se fait avec des aiguilles creuses de petit diamètre et est réservée aux tumeurs
- La macro-biopsie : elle doit être guidée par la mammographie ou l’échographie. Une anesthésie locale rend l’examen indolore. Les aiguilles utilisées (mammotome) sont plus grosses que pour la micro-biopsie. Elles permettent de prélever un fragment de tissu plus important. Elle sera préférée dans l’exploration de micro-calcifications. Dans ce cas un clip métallique sera posé afin de repérer la situation exacte de celles-ci dans le sein.
- La biopsie chirurgicale : elle permet une ablation partielle ou totale de la masse anormale ou des ganglions lymphatiques afin d’évaluer une éventuelle propagation. Cette technique est proposée quand la macro biopsie n’est pas faisable ou contributive. Elle est effectuée au bloc opératoire, sous anesthésie générale et nécessite une hospitalisation. Elle est de moins en moins pratiquée.
Les résultats de l’examen anatomopathologique
Ces résultats permettent de confirmer :
- Le type histologique, le plus souvent adénocarcinome (prolifération de cellules épithéliales glandulaires), soit canalaire ou de type non spécifique NST, soit lobulaire soit autre
- Le caractère invasif ou non (in situ ou invasif)
- Le grade (le degré d’agressivité de la prolifération tumorale, Grade I peu agressif à III très agressif, le grade II est intermédiaire)
- Il sera complété par la recherche par méthode immunohistochimique sur coupes effectuées à partir du matériel inclus en paraffine, des facteurs pronostiques ou prédictifs de la réponse à certains traitements : la présence de récepteurs hormonaux RE, RP (tumeur dite hormonosensible, RH+) et/ou la présence d’une surexpression de HER2 (tumeur dite HER2 positives) , indice de prolifération cellulaire Ki 67
- A l’issu de cette analyse, le résultat est adressé au médecin prescripteur. Il faut compter environ 1 semaine pour obtenir les résultats d’une biopsie 2 à 3 semaines pour une pièce opératoire.
3 – Le cas du cancer invasif
Dans le cas d’un cancer invasif, un bilan d’extension sera réalisé à la recherche de localisations secondaires. Ce bilan peut comporter une radiographie du thorax, une scintigraphie osseuse, un scanner, une échographie abdominale, ou une IRM. Un bilan sanguin complet est réalisé. Ces examens ne sont pas systématiques et seront prescrits en fonction de chaque cas.
À l’issu de ce bilan, on définit le stade de la maladie.
Ne pas confondre stade et grade !
-
Le stade
Le stade est, du point de vue clinique et/ou radiologique, l’état de la maladie. Il est évalué en fonction du TNM : T représente la taille et le degré d’envahissement local, N le nombre et la localisation des ganglions et M pour l’existence ou non de métastases.
-
Le grade
Le grade (1-2-3) est une donnée microscopique sur l’aspect des cellules, signant le degré d’agressivité de la tumeur.
Facteurs pronostiques et approches thérapeutiques
Certains paramètres sont analysés dans la prise de décision thérapeutique, car ils renseignent sur le risque de récidive après traitement.
- L’âge : plus la femme est jeune, plus la tumeur est agressive et de plus haut grade, plus le risque de récidive est accru,
- Certains types de cancers de seins infiltrants (carcinomes tubuleux, mucineux, médullaires et papillaires), risquent moins de se propager aux ganglions lymphatiques et engendrent un pronostic plus favorable,
- Le stade: plus le stade est bas, meilleur est le pronostic,
- Le grade: à un stade identique, plus le grade est bas, plus le pronostic est bon,
- Les tumeurs qui ne présentent pas de récepteurs et ne surexpriment pas Her2, dites « triple négatives, sont souvent plus agressives,
- La présence de récepteurs hormonaux signe une maladie moins agressive et peut bénéficier d’un traitement hormonal,
- La présence de signes inflammatoires signe une maladie plus agressive,
- Les tumeurs qui sur-expriment HER2 ont tendance à être plus agressives, souvent de plus haut grade et plus susceptibles de se propager à distance.
Les facteurs qui orientent vers une approche thérapeutique
- Les récepteurs hormonaux (récepteurs aux œstrogènes et récepteurs à la progestérone) : Les tumeurs qui expriment les récepteurs hormonaux pourront bénéficier d’un traitement hormonal,
- Les récepteurs HER2 : Les tumeurs qui surexpriment HER2 vont bénéficier d’un traitement par des anti-HER2 (Trastuzumab, par ex)
En fonction des différentes combinaisons possibles, voici des propositions de traitements :

Les tests génomiques prédictifs
https://youtu.be/PpVsu0ogXno
Cancer du sein et tests prédictifs
Pr Mario CAMPONE
À une question pas totalement nouvelle, mais toujours plus pressante «Est-il nécessaire de faire une chimiothérapie adjuvante, c’est-à-dire après la chirurgie, à toutes les patientes porteuses d’un cancer du sein hormonodépendant ? », Bernadette Carcopino, Gynécologue à Paris, et Patricia de Crémoux, Biologiste à l’Unité d’Oncologie Moléculaire de l’Hôpital Saint Louis, Paris, nous présentent les tests prédictifs qui apportent aujourd’hui une réponse de plus en plus précise et fiable.
1 – Sur quelles bases les tests moléculaires se sont-ils développés ?
Tous les tests utilisés aujourd’hui sont basés sur les travaux menés il y a une vingtaine d’années, notamment par Pierre Roux, sur l’ARN messager, support de l’information pour la synthèse des protéines, sur lesquelles vont agir les médicaments.
L’analyse de milliers de gènes a permis de regrouper les tumeurs du sein selon leur profil d’expression et d’établir ainsi leur classification intrinsèque moléculaire en 3 catégories : cancers basal-like, HER2-like et cancers luminaux ou hormonodépendants qui sur-expriment les récepteurs aux œstrogènes et à la progestérone et représentent les deux tiers des cancers du sein.
20 à 40% de ces tumeurs luminales sont définies à risque intermédiaire – entre le risque faible des tumeurs sans envahissement ganglionnaire, de bas grade, peu proliférantes, n’exprimant pas HER2 et justifiant une seule hormonothérapie et, à l’opposé, le haut risque des tumeurs à envahissement ganglionnaire, de grade plus élevé, proliférantes, exprimant peu les récepteurs aux œstrogènes et qui impose la chimiothérapie – et posent donc le problème de la stratégie adjuvante.
Parmi les tests disponibles, 3 sont utilisés majoritairement en France : Oncotype DX®, Prosigna® et Endopredict-EpClin®. Leurs différences résident dans le nombre de gènes analysés et la stratification du risque à respectivement 3, 3 et 2 niveaux (faible et haut).
2 – Dans quel contexte les tests moléculaires sont-ils indiqués ?
Les tests prédictifs sont prescrits en Réunion de Concertation Pluridisciplinaire (RCP) pour les tumeurs hormonodépendantes au stade précoce, HER2 négatives, T1 ou T2 ( jusqu’à 5 cm), sans envahissement ganglionnaire ou avec atteinte ganglionnaire microscopique.
Les données issues de ces tests sont colligées dans un recueil national.
3 – Quelles sont les modalités pratiques de réalisation des tests moléculaires ?
L’ARN est extrait, dans le cas du test EpClin®, d’un échantillon tumoral fixé dont la préparation est réalisée par l’anatomopathologiste.
L’analyse des 11 gènes, dont 3 de référence, associée à l’évaluation de la taille de la tumeur et du statut ganglionnaire permet d’établir un score EpClin® de risque, bas ou élevé.
4 – Quels résultats délivre-t-on aux cliniciens ?
Le rendu des résultats comporte la classification du risque EP (score prédictif moléculaire), les paramètres clinico-pathologiques (taille de la tumeur et statut ganglionnaire), la classification du risque selon le score EpClin – qui intègre les données précédentes – et la détermination de la probabilité d’une rechute à distance.
En dessous d’un score EpClin de 3, 33, le risque est faible, au-dessus il est élevé.
5 – Que coûtent les tests moléculaires et comment sont-ils pris en charge ?
Les tests prédictifs ont un coût élevé, autour de 1 500€ par test.
Ils sont aujourd’hui pris en charge dans le cadre du dispositif RIHN (Référentiel des actes Innovants Hors Nomenclature) qui en permet l’accès dans l’attente de l’évaluation menée par la HAS sur la base des données recueillies. Cette disposition semble cependant incertaine.
Conclusion
Tout l’intérêt des tests prédictifs réside dans l’aide qu’ils apportent à la décision thérapeutique.
Lorsqu’ils excluent la chimiothérapie, ils offrent le bénéfice immédiat d’une meilleure tolérance du traitement et le bénéfice à long terme de l’absence des effets indésirables de la chimiothérapie.
Ils permettent aux cliniciens, grâce à une évaluation plus précise du rapport bénéfice/risque, de trouver l’optimum pour la patiente, d’altérer au minimum la qualité de vie, voire de préserver le pronostic vital lorsque la thérapeutique peut s’avérer plus lourde que la maladie elle-même.
Les tests moléculaires constituent, pour les patientes porteuses d’un cancer du sein hormonodépendant comme pour leurs médecins, un progrès qui permet la désescalade thérapeutique lorsqu’elle est possible.
En conclusion...
C’est à l’issu de l’ensemble de ce bilan que le diagnostic est posé et la stratégie thérapeutique sera discutée en réunion de concertation pluridisciplinaire (RCP). La proposition du traitement sera faite à la patiente au cours de la consultation d’annonce, par le médecin référent, le plus souvent l’oncologue. Les objectifs et les effets secondaires du traitement seront détaillés, et l’acceptation de la patiente validée avec l’organisation de parcours personnalisé de soin (PPS).